광여기 이탈법의 원리
광여기 이탈은 세 가지 과정 (①광여기, ➁결합 절단, ③이탈)
①광여기
σ 궤도(결합성 궤도)의 전자는 σ 궤도와 σ* 궤도의 에너지 차이에 대응하는 파장의 빛을 흡수하면 σ* 궤도(반결합성 궤도)에 여기됩니다.
광속 밀도가 높은 진공 UV를 사용함으로써, 광로가 짧은 박막에서도 효율적으로 시료를 여기합니다.
②결합 절단
σ 궤도와 σ* 궤도 각각에 하나의 전자가 있는 경우 결합 에너지는 두 궤도 레벨의 합계입니다. 결합 에너지가 음수이면 σ 결합은 절단됩니다.
③이탈
σ 결합이 절단되면 다양한 단편이 생성됩니다. 일부 분자에서는 표면에서 재결합이 발생합니다. 생선된 단편이 시료중에 속박되어 있지 않은 경우에는 이탈이 일어납니다.
다음에 이것을 포텐셜 곡선으로 설명하겠습니다.
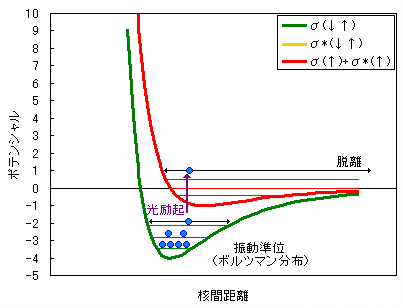
그림1 포텐셜 곡선
2개의 전자가 결합성궤도에 있는 상태(그림 1의 포텐셜 곡선은 녹색)에서는,
이 결합에 전자천이를 일으키는 파장의 진공자외선이 닿으면、결합성괘도와 반결합성괘도에 1개씩 전자가 있는 상태(그림1 적색 포텐셜 곡선)이 됩니다.
제로 이상의 포텐셜에너지에 있는 분자는 결합이 분리됩니다.
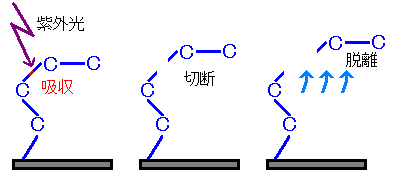
그림2 진공자외선에 의한 절단
한편、다중결합이나 단편이 속박되어 있는 경우 、결합이 완전히 절단되지않거나 、절단되어도 분리되지 않는 경우가 있습니다.
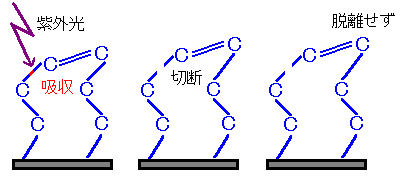
그림3 절단되어 있으나 이탈 불성립의 경우①
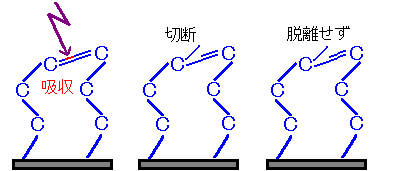
그림4 절단되어 있으나 이탈 불성립의 경우②
